Kam směřuje vývoj nových inzulinových pump: uplatní se bihormonální systémy?
Pracoviště: Klinika diabetologie, IKEM Praha
Vloženo: 12. 3. 2021
Pravda, něco takového už tu je. Nový pankreas od zemřelého dárce nebo transplantované Langerhansovy ostrůvky se dovedou postarat. Mají přirozenou schopnost produkovat inzulin přesně podle potřeby. Umějí spustit, když si dáme pořádně do nosu, nebo dát si pauzu, když se nám jíst nechce. Ale takový pankreas nebo ostrůvky pocházejí od zemřelého dárce orgánů, který musí splňovat řadu podmínek. Transplantace není jednoduchá, a navíc je po jejím provedení nutné trvale užívat imunosupresivní léky. Česká republika sice v tomto ohledu stojí v přepočtu provedených transplantací na počet obyvatel v čele Evropy, ale i tak se zde provádí jen asi 50 výkonů ročně. A pacientů s diabetem 1. typu je u nás možná víc než 60 000.
Až teprve nyní, plných 100 let po objevení inzulinu, přicházejí oficiálně noví pomocníci. Jako skutečné beta-buňky pankreatu to sice ještě zdaleka neumějí, ale zato se dají průmyslově vyrábět. Díky tomu schopné a odhodlané osoby s diabetem 1. typu, které mají dostatečný přístup k léčebným prostředkům, mohou nyní udržovat glykémii během dne i noci v rozmezí, které je už dost blízké normálním hodnotám.
Zmiňovanými pomocníky jsou tzv. hybridní polouzavřené systémy. Ty zahrnují 1) kontinuální monitor hladiny glukózy v podkoží (senzor), 2) inzulinovou pumpu a 3) řídící algoritmus, který je uložen v operačním systému pumpy nebo v jiném mobilním zařízení, např. telefonu. Senzor komunikuje v reálném čase s inzulinovou pumpou, která je řízena příslušným algoritmem a díky němu je schopna zvyšovat nebo snižovat rychlost aplikace inzulinu, případně jeho podání dočasně zastavit. Systém sice stále vyžaduje občasné kontroly pacientem, nastavení správných citlivostí na inzulin a inzulin-sacharidových poměrů a ruční zadávání správného množství sacharidů před každým jídlem, ale když se to pacient dobře naučí, může většinou v noci klidně spát a ráno se probudí s krásnou glykémií. Tyto systémy i nadále umožňují „ruční” volbu příslušných bolusových dávek.
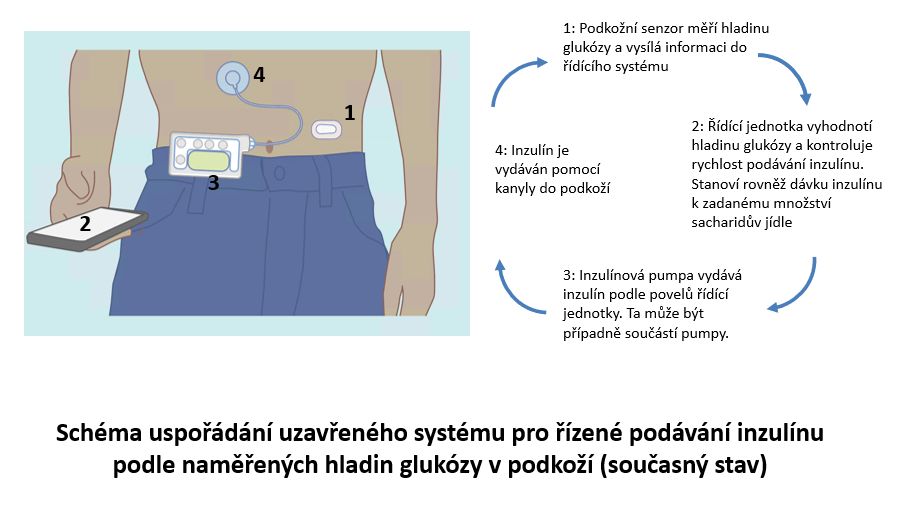
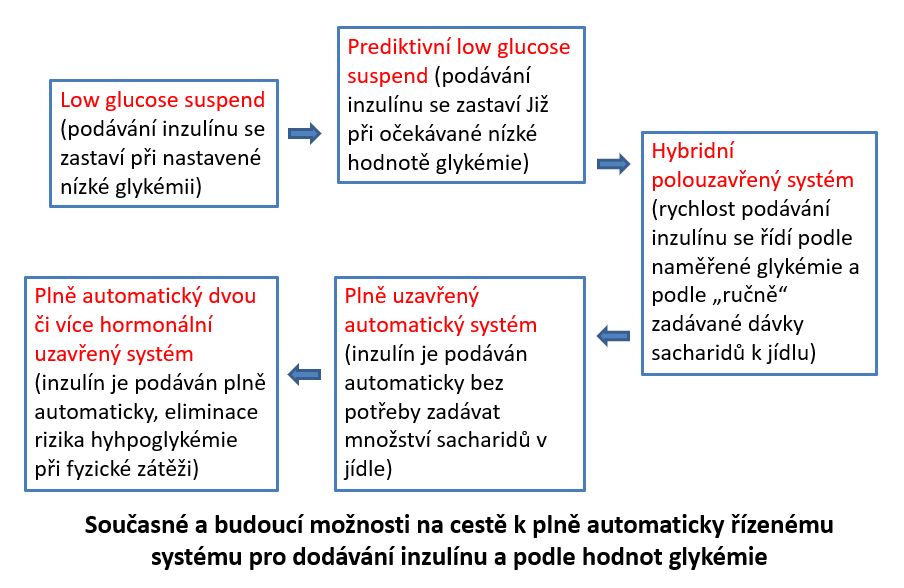
Přestože myšlenka (polo)automatického podávání inzulinu na podkladě naměřených glykémií je stará už 50 let, hlavní překážkou pro její realizaci byly nedokonalé metody pro spolehlivé kontinuální měření hladiny glukózy. Další technické problémy spočívaly v nemožnosti dostatečně miniaturizovat potřebnou výpočetní techniku, která by navíc bezdrátově komunikovala se spolehlivou inzulinovou pumpou na odpovídající technické úrovni.
Jednotlivé obtíže byly postupně překonávány a již před několika lety se do praxe dostaly inzulinové pumpy, které dokáží při hrozící hypoglykémii včas přerušit aplikaci inzulinu (tzv. low suspend technologie). Technologie postoupila zase o krůček dál a v tomto okamžiku jsou v ČR na oficiálním trhu již dva výše zmiňované hybridní polouzavřené systémy, které kromě funkce low suspend (zastavení aplikace inzulinu při hypoglykémii) dokáží automaticky zpomalovat či zrychlovat podávání inzulinu, případně automaticky vydávat korekční bolusové dávky. V ČR jsou zatím dostupné dva systémy (Medtronic 780G a Tandem Control IQ). Řada studií ukázala, že tato zařízení u dobře spolupracujících pacientů zlepšují kompenzaci diabetu a snižují výskyt hypoglykémií, a to nikoliv na úkor pohodlí pacienta. Ten se naopak cítí bezpečněji a část starostí může přenechat technologii. Zejména v nočních hodinách, kdy odpadá riziková kalkulace bolusových dávek před jídly nebo variabilita účinku inzulinu při námaze, tyto systémy příjemně udržují doporučené hodnoty glykémií. Je třeba také zmínit, že ve světě někteří pacienti již léta používají neoficiální uzavřené systémy, které nejsou vyráběny žádnou schválenou technologickou firmou, ale byly vymyšleny a sestaveny z dostupných dílů samotnými uživateli, kteří mají diabetes a zvládají složité elektronické technologie. Jedná se o tzv. „udělej si sám systémy – do it yourself“, které v mnohém předbíhají dobu, ale nejsou z hlediska zdravotnické legislativy schválené, a lékaři je tedy nemohou doporučovat.
Současné hybridní systémy však mají stále své limity. Mezi technické limity stále patří někdy nedostatečná přesnost měření glykémie pomocí senzorů (měření je prováděno v mezibuněčné tekutině v podkoží), příliš dlouhý účinek inzulinu aplikovaného do podkoží a jeho ne vždy pravidelné vstřebávání do krevního oběhu, nedostatečná regulace glykémií po jídle (při špatně spočítaném množství sacharidů, špatném nastavení citlivosti na inzulin či inzulin-sacharidových poměrů nebo při chybně kalkulovaném ručním bolusu). Pokud usilujeme o udržování glykémií opravdu velmi blízko normálním hodnotám, narážíme na problém zvýšeného rizika hypoglykémií, které mohou vznikat při fyzické námaze.
Aby se co nejvíce omezilo riziko pozdních komplikací diabetu a zároveň pacient nebyl ohrožen hypoglykémiemi, doporučují Česká i Evropská diabetologická společnost udržovat glykémie v rozmezí 3,9 – 10 mmol/l alespoň během 70 % (ale raději v 80 %) veškerého času. Méně než 4 % času by měl diabetik strávit v oblasti pod 3,9 mmol/l a méně než 1 % času pod 3 mmol/l. Obecně platí, že u většiny pacientů jsou hypoglykémie jedním z hlavních limitů pro dosažení tohoto cíle. Hybridní systémy výraznou měrou přispívají ke zlepšení kompenzace diabetu a zjednodušují pacientovi život, ale ani ony nemusí dokázat hypoglykémiím předejít, a to zejména při fyzické námaze. Důsledkem snahy předejít hypoglykémii je často hyperglykémie, která se objeví buď před situací, která by k hypoglykémii vedla, nebo po této situaci.
U zdravého člověka jsou kontraregulační reakce při hrozící hypoglykémii značně komplexní a zahrnují jak řídící povely ze strany centrálního nervového systému, tak vyladěnou reakci humorální. První a zcela zásadní reakcí je snížená nebo téměř zastavená produkce inzulinu, jehož doba účinku je při fyziologickém uvolňování do portálního řečiště v řádu minut. Následuje reakce glukagonu, který stimuluje jaterní fosforylázu a uvolňování glukózy z glykogenu. Před hlubší hypoglykémií zásadně chrání adrenalin s podobným efektem, jehož sekrece je řízena centrálně.
Zejména první dva mechanismy jsou však zcela odlišné u pacientů s diabetem 1. typu. Inzulin se podává „uměle” do podkoží a jeho vstřebávání může (i po ukončení podávání) pokračovat i několik hodin. Alfa-buňky pankreatu, které normálně produkují glukagon, jsou sice zachované, ale jejich reaktivita při chybění sousedního protihráče v podobě beta-buněk je brzy po vzniku diabetu 1. typu zpomalená. Z látek reagujících na hypoglykémii nám tedy zbývá adrenalin. Jeho zvýšená sekrece vyvolává vedlejší příznaky (třes, bušení na hrudi…), které diabetika často na hypoglykémii upozorní. Je důležitý pro rozpoznávání hypoglykémie. Tedy pokud není i tato reakce částečně vyřazena v důsledku autonomního vegetativního selhávání…
Nebezpečí hypoglykémie naštěstí do značné míry snižují systémy kontinuálního monitorování glykémie, které pacienta pomocí správně nastavených alarmů varují. Ve spojení s inzulinovou pumpou mohou navíc včas podkožní infuzi inzulinu zastavit (výše zmiňovaná funkce „low suspend“) a poté zase obnovit. I tak ale zůstávají hypoglykémie zatím nerozlučným partnerem diabetika léčeného inzulinem.
Obzvlášť těžké je hypoglykémiím předcházet v průběhu delší fyzické zátěže a ještě několik hodin po ní. Preventivně se nabízí včasné zastavení/zpomalení podávání inzulinu, či příjem sacharidů před zátěží nebo v jejím průběhu. Chyby se ale trestají, nejčastěji v podobě těžší hypoglykémie, která nejen že fyzickou aktivitu zcela naruší, ale později zpravidla vede pro změnu k hyperglykémii. Přílišná redukce dávky inzulinu (resp. nadměrný příjem sacharidů) může mít zase za následek vysokou glykémii či počínající ketózu po ukončení zátěže.
Tyto problémy by mohla v budoucnosti řešit inzulinová pumpa zapojená do řízeného okruhu spolu se senzorem glykémií, která by kromě inzulinu byla schopna vydávat také glukagon.
Do současné doby bylo testováno již několik takových systémů, z nichž některé mají blízko k povolovacímu řízení pro klinické použití. Dosud byla velkým problémem malá stabilita glukagonu, který na rozdíl od inzulinu vyžadoval každodenní přípravu pro naplnění pumpy. Nově však byl připraven glukagon, který zůstává v zásobníku pumpy stabilní stejně jako inzulin.
Tzv. bihormální pumpy s polouzavřeným hybridním systémem kontroly glykémií vydávají podle nastaveného algoritmu inzulin. Pokud ale systém vyhodnotí, že navzdory přerušenému podávání inzulinu dojde v průběhu 5 – 15 minut k hypoglykémii, podá systém oddělenou kanylou do podkoží malé dávky glukagonu, který hypoglykémii zabrání. Může k tomu dojít např. v průběhu náročnější fyzické zátěže, nebo pokud pacient špatně odhadne množství sacharidů v jídle, a dávka inzulinu je příliš vysoká. Několik studií již potvrdilo, že tímto způsobem se výskyt hypoglykémií výrazně sníží, což pacientům pochopitelně přináší nejen lepší dlouhodobé výsledky, ale zejména klid. Ve stadiu testování jsou nyní již integrované pumpy se dvěma oddělenými okruhy pro inzulin a pro glukagon. Jsou ale pochopitelně složitější a využívají dvě oddělené kanyly zavedené do podkoží.
Plně automatické systému pro regulaci glykémie u osob s chybějící sekrecí inzulinu zůstávají zatím v reálném světě iluzí. Především by pro ideální přesnost bylo nutné měřit hladinu glykémie přímo v krevním řečišti, a nikoliv v podkoží. Rovněž inzulin by se měl mnohem rychleji dostávat do krevního řečiště a měl by mít jen velmi krátký účinek, jak je tomu u zdravých osob. Zařízení by mělo prakticky okamžitě rozpoznat příjem sacharidové potravy a mělo by také reagovat na zvýšenou tělesnou aktivitu. Něco podobného je zatím možné jen v čistě laboratorních podmínkách, kdy se vyšetřovaná osoba chová naprosto standardně podle naprogramovaného protokolu, glykémie se měří přímo v žilním řečišti a inzulin se rovněž podává nitrožilně. Podobné zařízení se někdy nazývá biostator a používá se k výzkumným účelům. Pro reálný život je však zatím nepoužitelné.

